
令和2年12月5日
京都府医師会館

総合司会
京都大学
小倉 雅仁 先生

講演1
久留米大学
室谷 健太 先生

講演2
二田哲博クリニック姪浜
下野 大 先生
久留米大学 バイオ統計センター 准教授
室谷 健太 先生
臨床研究を読み解いていく上で、統計学は計画・解析・解釈の全てにおいて本質的に寄与する学問の1つである。ランダム化比較試験や、流行りのリアルワールドデータ解析においても統計学的な視点を持って結果を読み解くことの重要性はこれまで以上に高まってきている。本稿では実例を挙げ、統計学的な視点から臨床論文を読み解くときのポイントについて考察していきたい。
注射と経口で効果が異なる?直感的に合わないランダム化比較試験を読み解く
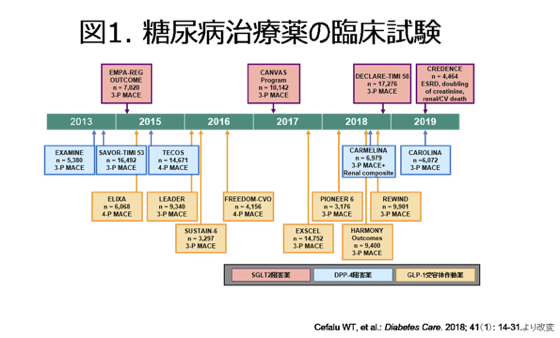
2型糖尿病治療薬の大規模ランダム化比較試験は図1のように数多く行われている([1]を一部改変)。
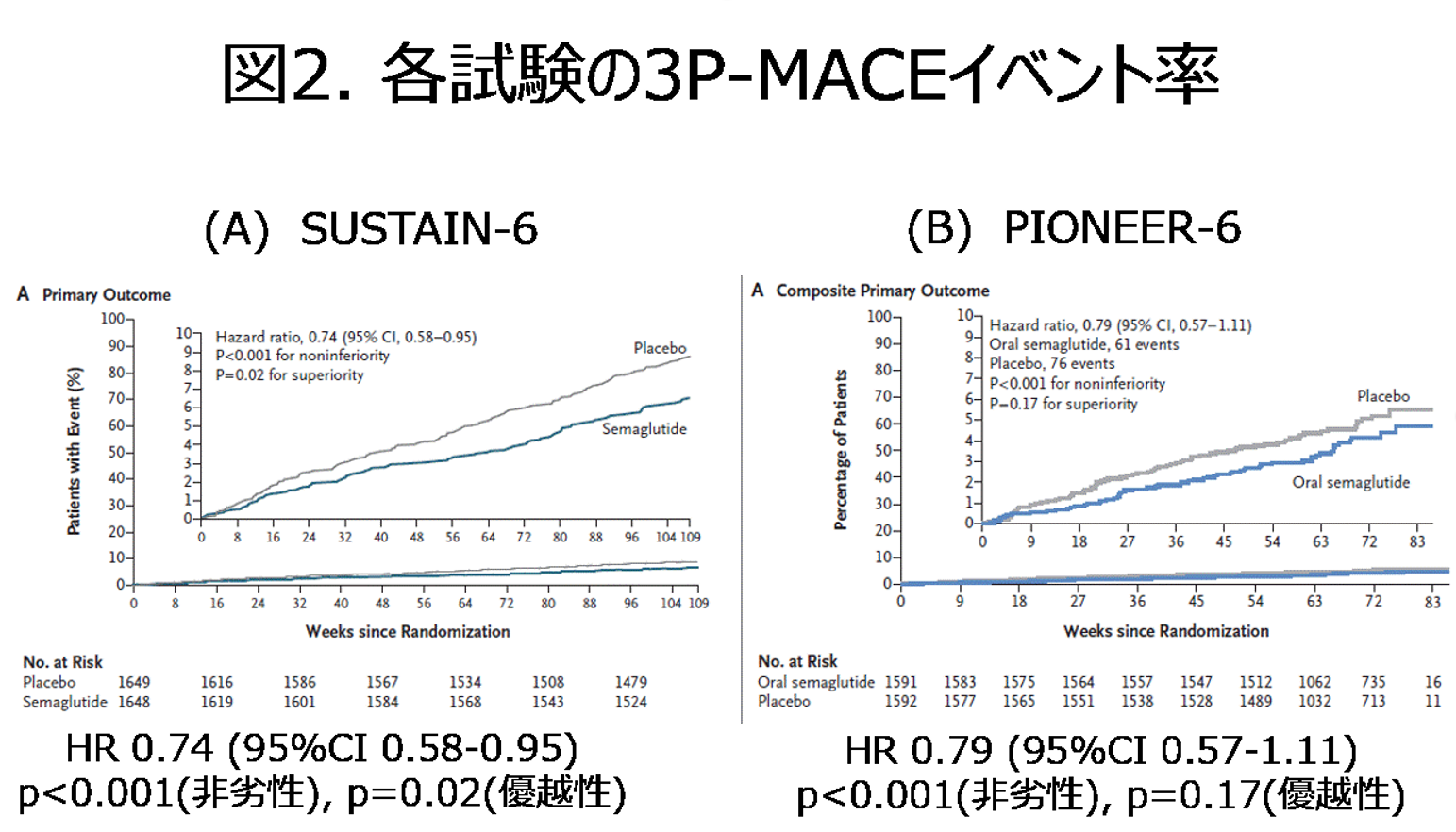
ここではGLP-1受容体作動薬に関する2つの大規模ランダム化比較試験、SUSTAIN-6とPIONEER-6試験について考えたい。SUSTAIN-6 [2]はGLP-1注射薬(国内:オゼンピック皮下注)のプラセボ対照試験、PIONEER-6 [3]はGLP-1経口薬(国内:リベルサス錠)のプラセボ対照試験である。いずれの試験も3P-MACE(心血管死、非致死性心筋梗塞、非致死性脳卒中のうち最も早くしたものをイベントとしたtime to event型の評価項目)を評価項目とした非劣性マージン1.8の非劣性試験として計画・実施された。どちらも非劣性が示された場合、続いて優越性も検証するデザインであった。主要評価項目の結果は図2のようになった。
結果を要約すると、注射薬(図2(A))はHR 0.74(95%CI: 0.58-0.95), p<0.001(非劣性), p=0.02(優越性)となり、プラセボに対するGLP-1注射薬の非劣性と優越性がどちらとも証明された一方、経口薬(図2(B))は、HR 0.79 (95%CI: 0.57-1.11), p<0.001(非劣性), p=0.17(優越性)となり、プラセボに対するGLP-1経口薬の非劣性は示されたが、優越性は示されなかった、という結果であった。両者は本質的には成分が同じであるため、直感的には注射でも経口でも、治療効果に差異はないことが期待されるが、注射は優越性が示され、経口は優越性が示されなかった。このことは、治療効果が注射薬の方が経口薬よりも強いことを示しているのだろうか?このような直感的に解釈が困難な結果が得られたときに統計的にはどういう考察が可能か列挙してみたい。
臨床試験に参加した患者が同じといえるかどうかは重要なポイントである。例えば、ある試験には高リスクの患者ばかりいて、もう一方の試験には低リスクの患者ばかり集まっていたり、重要な予後因子に関する条件が片方には考慮されているが、もう片方には考慮されていなかったり、などといった点である。
<過去の臨床試験から1つ例を挙げてみよう。SGLT2阻害薬の効果を検証するための第3相プラセボ対照ランダム化比較試験であるEMPA-REG OUTCOME試験[4]とCANVAS試験[5]における心血管死の結果の相違がこれに対応するであろう。EMPA-REG OUTCOMEではプラセボに対してEmpaglifrozinの心血管死のHRが0.62 (95%CI 0.49-0.77)であったのに対してCANVAS試験(Canagliflozin)でのそれは0.87 (95%CI 0.72-1.06)であった。どちらもSGLT2阻害薬であるのでそこまで違いは生まれなさそうであったが、集団を見てみるとEMPA-REG OUTCOMEは2次予防の患者が100%の集団であり、CANVASは2次予防70%、1次予防30%であった。もしかすると1次予防の患者集団では心血管死リスクが2次予防患者集団よりも低く、そのせいで心血管死のHRの差異が生じたのかもしれない。もちろんこれは1つの仮説であり、当時は様々な視点から喧々諤々の議論が行われていたことにも注意されたい。
さて、SUSTAIN-6とPIONEER-6に話を戻そう。集団の定義を調べたいときは適格基準と除外基準を見比べることで把握することが可能である。理想はプロトコルの適格基準、除外基準を確認することである。論文のSupplementaryにプロトコルが掲載されていれば容易に確認できるが、そうでない場合は、論文中の記載を読み取るしかない。ただ論文中には主な基準しか記載されていないことも多く、可能であれば製薬会社担当者などを通じて詳細な情報を得た方がよいだろう。なお、SUSTAIN-6とPIONEER-6の両試験の適格基準、除外基準を確認してみると試験結果に大きな影響を与えそうな差異はなかったように思われる。このパラグラフにおける大事なポイントは、直感的に結果に違和感あるときは、「そのエビデンスは誰のものなのか?」という原点に戻って考えることである。
次に確認したいポイントは対照群の成績についてである。SUSTAIN-6とPIONEER-6のどちらもプラセボ対照試験であり、かつ、前項の考察から適格基準、除外基準もほぼ同じであることから、偽治療であるプラセボ群の治療成績は両者で同じような結果となることが期待される。この点を確認しておこう。
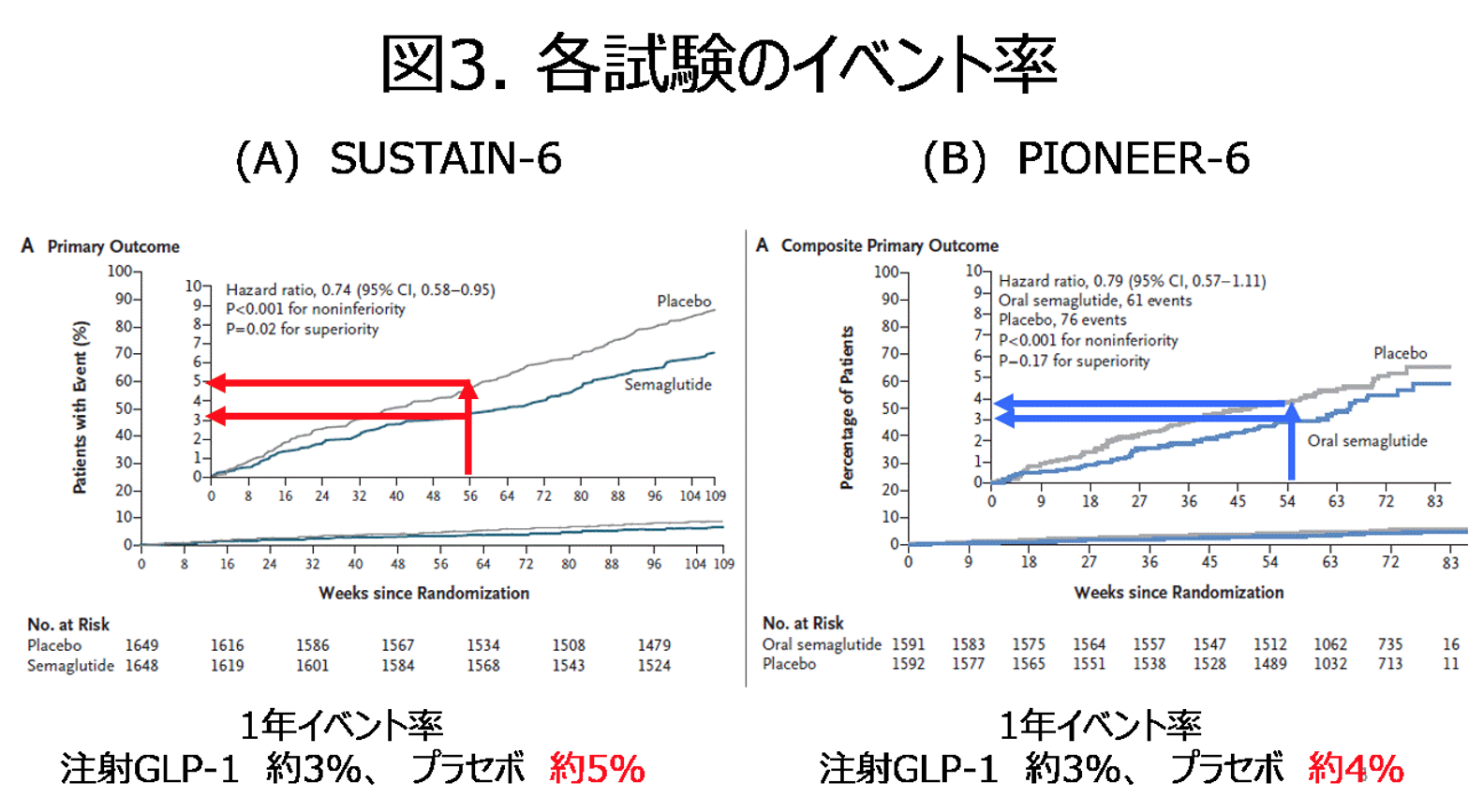
図3は各試験の3P-MACEのイベント曲線を示したものである。比較しやすいようにここでは1年イベント率を使って両者の差異を調べてみよう。するとSUSTAIN-6はGLP-1注射薬群で約3%、プラセボ群で約5%であったのに対して、PIONEER-6はGLP-1経口薬群で約3%、プラセボ群で約4%であった。ワンポイント(1年時点)での数値ではあるが、試験治療群の成績はどちらも同じであるが、プラセボ群は若干SUSTAIN-6の方が、イベント率が高いようである。
3P-MACEのようなエンドポイントの場合、結果は一般的にハザード比で表現される。この「比」という尺度が統計学ではたびたび用いられるが、厄介な代物である。SUSTAIN-6のHR=0.74とPIONEER-6のHR=0.79という数値だけ見ると、PIONEER-6の方が、HRが1に近いため試験治療群の効果が弱いように見えてしまう。しかし1年イベント率で見てみると試験治療群の成績は同じで、プラセボ群にのみ差異があっただけである。これはもしかすると実は試験治療の効果は同じで、たまたまプラセボ群の治療成績が違っていただけで我々はないはずの差異を見てしまったのでは?と考えることは出来ないだろうか。統計では誰かと比べることで評価することが多いので、直感的に違和感があるときは「誰に比べてどうだったのか?」という視点から考察することは有益であろう。
私はここでGLP-1注射薬とGLP-1経口薬の効果が同じだと言いたいのではないことは申し添えておきたい。臨床試験の数値を鵜呑みするのではなく、どういう設定の下でそのデータは生まれてきたのか?を考察することの重要性を言いたいのである。本稿で述べた「そのエビデンスは誰のものか?」「対照群の成績はどうだったのか?」に留意して結果を眺めてみると新たな発見があるかもしれない。
昨今、リアルワールドデータ(Real World Data; RWD)という単語に触れる機会が多くなったように思う。一昔前まではレトロスペクティブ研究とか後方視的研究などと称され、どこかエビデンスレベルが一段落ちた研究であるように扱われていたが、ものは言いようである。そもそも何故リアルワールドデータの重要性は増してきたのだろうか。まずはランダム化比較試験(Randomized Controlled Trial; RCT)との違いを確認しておこう。RCTはランダム化を行い、厳密に適格基準、除外基準を規定して新治療の効果を調べる実験的研究であるのに対して、RWDは実臨床行為に基づくデータベースに蓄積されたデータを用いて適切な統計解析を施すことで実臨床のエビデンスを得るための研究である。RCTは厳密な薬効評価、RWDは実臨床のエビデンス、という棲み分けがあることを知っておきたい。
今も昔もエビデンス構築の基本はRCTであることは間違いない。RCTはランダム化によって比較可能性を高め、(一般に第3相試験であれば)全世界から症例を集積し、用法用量も厳密に規定することで「真にその治療に効果があるかどうか」に対して最善解を与えることの出来るおそらく唯一の方法である。ただ、厳密であるがゆえに、例えば超高齢者や腎機能が落ちている患者など適格基準、除外基準に抵触した患者集団のデータは含まれていないし、全世界から症例集積しているため日本人でも同じ結果となるのかどうかも分からない、さらに決まった用法はあるもののその通り使わない患者だって実臨床ではいるはずである。すなわち、薬が承認された後、実臨床における患者像とRCTに参加した患者像には隔たりがあるのである。リアルワールドデータ解析はRCTでは調べることの出来ない実臨床におけるエビデンスを補完してくれる存在という見方も出来るであろう。
Seino et al.は東アジア3カ国(日本、韓国、台湾)の約57000人の成人2型糖尿病患者の実臨床におけるデータを集積し、DPP4阻害薬を対照としたEmpaglifrozinの実臨床における効果を検討した[6]。結論を要約すると、DPP4阻害薬と比較してEmpaglifrozinの心不全入院、末期腎不全、全死亡リスク低下と相関しているという結果であった。
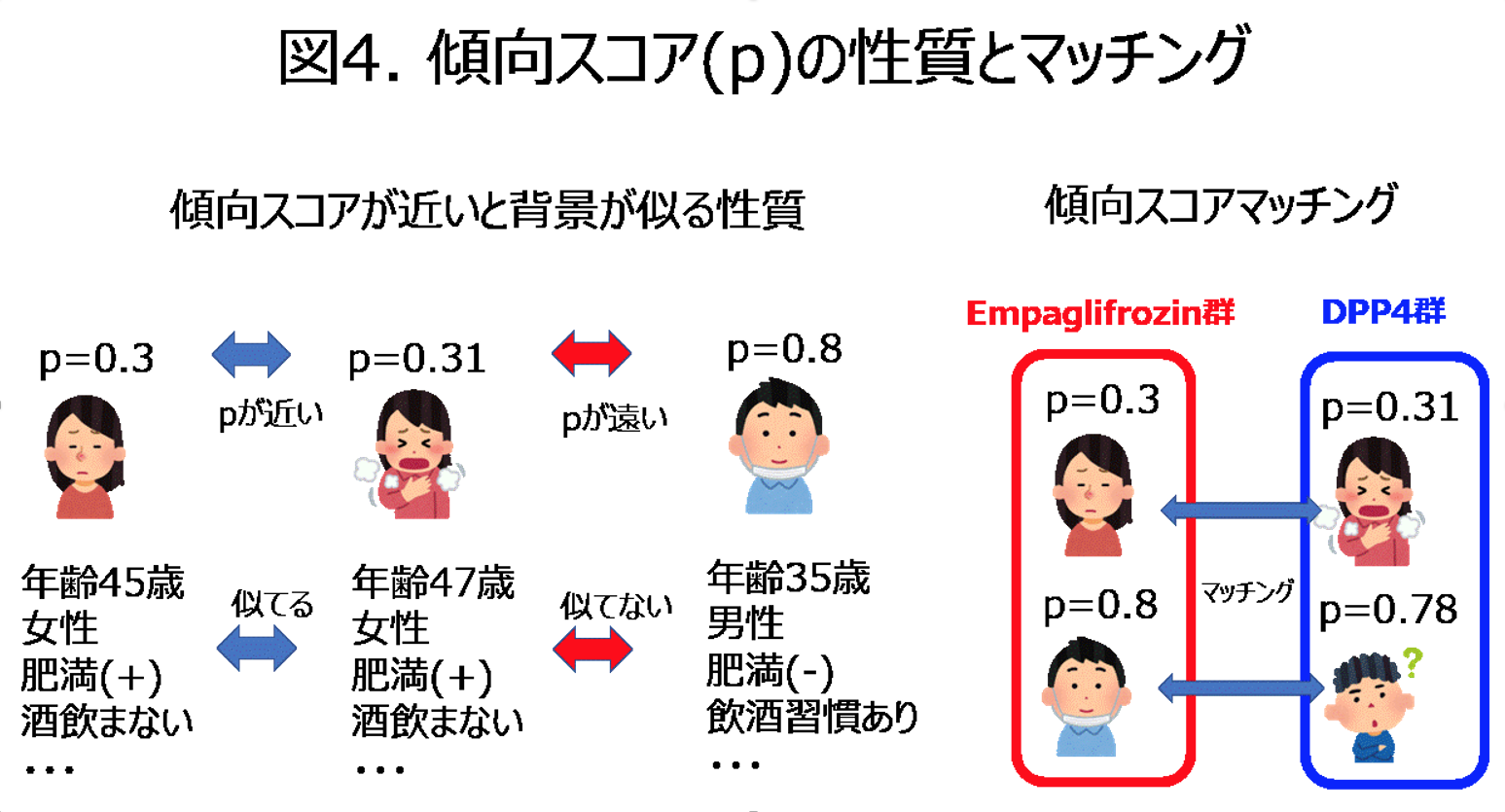
この論文では傾向スコアマッチング(propensity score matching)を用いている。傾向スコアはリアルワールドデータを用いた2群比較において頻用されている。傾向スコアとは今の文脈でいえばEmpaglifrozinを処方される確率のことである。図4に傾向スコアが持つ特徴を図示した。一言でいえば傾向スコアが近い患者の特徴(患者背景)は似る性質があるので、Empaglifrozin群とDPP4群の間で、傾向スコアが近い症例をマッチングすると、患者背景は同じで治療法だけが異なる2群となることが期待できる。
傾向スコアを使った論文を読み解く際に注意したいポイントは、1)どんな共変量を使って傾向スコアを推定しているか? 2)マッチング前後の群間の偏りが改善しているか?である(もっと細かく情報は[7]や[8]を参考にされたい)。
まず1)についてである。傾向スコアは比較したい2群の治療が処方される確率であると述べたが、この確率は目的変数を治療群としたロジスティック回帰や機械学習法を利用して推定されることが多い。ここで大事なことは、どの方法で推定したかよりも、何を共変量(説明変数)にしたかの方である。解釈上では、傾向スコアを推定するモデル式に投入した共変量については比較群間のバランスはとれていると解釈されるが投入されていない変数はバランスが無視されていると解釈される。そのため、共変量のリストを論文中から読み取り、比較する上で医学的に大事な変数が網羅されていることをチェックすることが肝要である。もし、決定的に重要な変数が入っていなければ、その比較の妥当性は怪しいことになるので、ここのチェックは重要といえる。なお、Seino et alでは130-149個もの共変量を用いて傾向スコアが推定されており、十分すぎるほどバランスを取っていた。症例数が十分大きいいからこそ出来たことでもあろう。
次に2)である。傾向スコアでマッチングする目的は患者背景を揃えることにあった。であれば、マッチングする前と後できちんと患者背景が揃ったことを統計学的に確認することが重要である。一般には標準化差(standardized difference)という尺度を用いて、それがマッチング後にはいずれも十分小さくなっていることを確認することが求められる。例えば標準化差0.1未満などが基準として用いられることが多いようである。たまにマッチング後の2群比較のp値を算出して、それが1に近いことをもってバランスを確認しようとする論文もあるが、このアプローチはあまりよくない。p値が大きいことは「差がないとはいえない」ことを示しており、差があるのかないのか断言できないからである。標準化差を用いて定量的に群間バランスを確認し、バランスが取れていることを確認してから比較の解析を行うことが大事である。
十分な症例数に基づき、医学的に重要な共変量を網羅した上で傾向スコアを推定し、マッチング後は標準化差でバランスチェックを行う。そこまでした後で、2群比較を行っていけばリアルワールドデータに基づく実臨床エビデンス(Real World Evidence)として臨床試験を補完する結果となるであろう。
本稿では臨床試験の結果解釈と、リアルワールドデータ解析の解釈における統計学的ポイントについて概説を試みた。実際のデータは教科書とは異なり、解釈に難渋するような結果と直面することも多い。本稿で述べた視点が今後の臨床研究結果の解釈に一助となれば望外の喜びである。
参考文献二田哲博クリニック姪浜 院長
下野 大 先生
今回の学術講演会のテーマは「糖尿病診療のエビデンスとエクスペリエンス」です。私からは新型コロナウイルス感染症対策を含めた、今実践している糖尿病診療の「エクスペリエンス」についてお話ししようと思います。
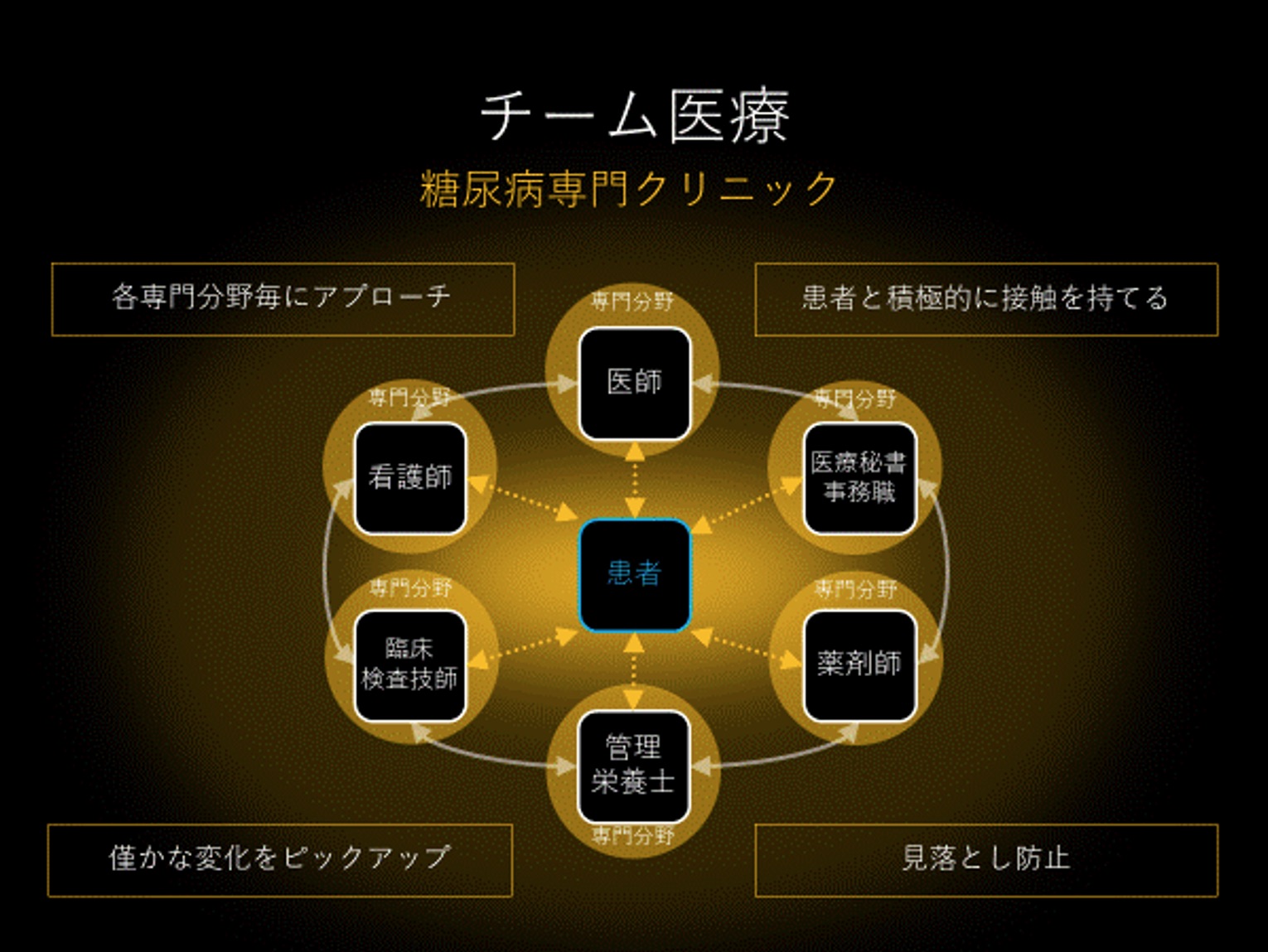
糖尿病診療においてチーム医療は重要です。チーム医療を行うことによって、診療の質の向上やスタッフのモチベーション向上、見落としの防止など、さまざまなメリットを得ることができます(図1)。中でも事務職は患者さんと最初と最後に接する職種であることから、患者さんの些細な変化に気付いてくれることも数多くあります。私たちの実践するチーム医療においては、それぞれの職種が時短や手技の精度・正確性を意識し、職種間のスムーズな情報伝達を心がけるようにしています。
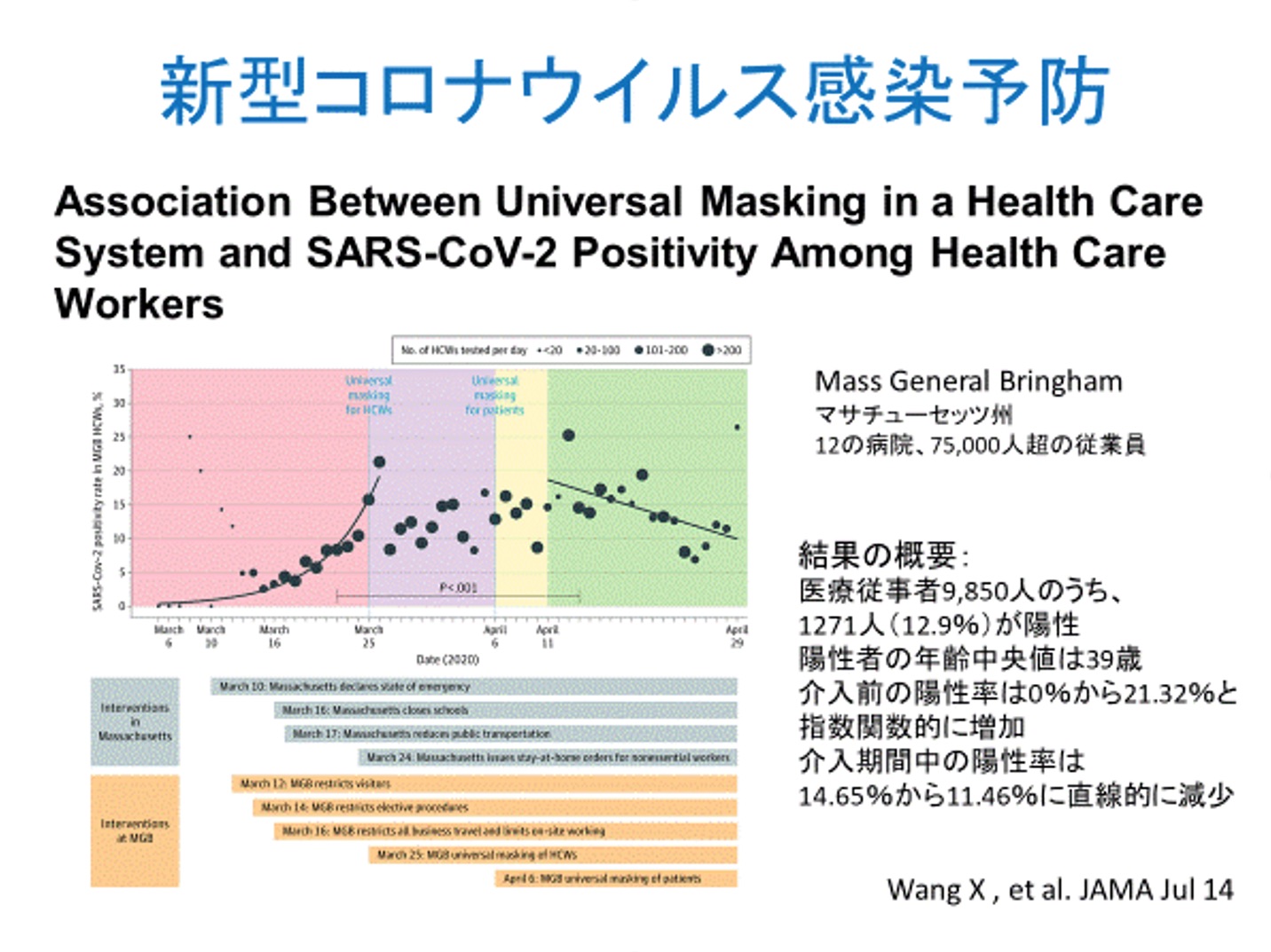
さて、糖尿病の外来診療において、その中で行われる医療行為の多様化がすすんでいることと併せ、ドロップアウト防止のための診療支援や待ち時間短縮も必要です。そのような中、2020年は新型コロナウイルス感染症対策も行う必要性が生じ、診療スタイルが一変しました。コロナウイルス感染対策としてPhysical distancingとマスクの着用が有効であることがSARS・MARSを併せたコロナウイルス感染症に関わる44研究のメタ解析で報告されており(図2)、新型コロナウイルス感染症対策としてUniversal Maskingが有効であることが報告されています(図3)。マスク着用によってお互いの表情が読み取りづらいなどのデメリットもありますが、やはり可能な限りの身体的距離の確保とマスクの着用は、現在の私たちの日常診療において必要なのだと考えられます。

糖尿病と新型コロナウイルス感染症の関係はどうでしょうか。新型コロナウイルス感染者における糖尿病患者の割合と糖尿病の有病率に差がないことから、糖尿病があるからといって新型コロナウイルス感染症に罹患しやすいわけではないものの、糖尿病は同感染症の重症化リスクになることが報告されています(GR Fadini et al. Journal of Endocrinological Investigation Mar 2020)。また、同感染症の重症化については、血糖コントロールが悪い場合に重症化のリスクが高まることが報告されています(L Zhu et al. Cell Metabolism Jun 2020)。そして、世界各国で行われているロックダウンによって、食事や運動などの生活習慣が変化することも分かっています(Di Renzo et al. J Transl Med (2020) 18:229)。新型コロナウイルス感染症対策が必要とされる現在、患者に正しい情報を提供し、個々の生活習慣の変化に対応した治療選択が必要になるものと考えられます。
運動については高齢化や感染症対策による不活動がサルコペニアにつながらないよう注意をする必要があります。また、食事についても適切なエネルギー摂取と蛋白質摂取が必要であり、高齢者において蛋白質の摂取量が少ないとADLやQOLが低下する可能性も示唆されています(Houston DK, et al. J Am Geriatr Soc. 65:1705-1711, 2017)。
薬物療法は、糖尿病治療ガイドにおいて2型糖尿病治療における治療薬の記載が変わりました(日本糖尿病学会編・著:糖尿病治療ガイド2020-2021)。また、この治療ガイドの中で糖尿病治療の目標も変更されており、サルコペニア・フレイルを予防する重要性、スティグマを除去することの重要性を改めて認識させる内容となりました。2020年4月に改訂された糖尿病連携手帳第4版においてもサルコペニア予防を意識した記載項目の追加がなされており、先生方の実臨床にぜひお役立ていただければと存じます。
一般社団法人 京都府歯科医師会 医療保険・介護保険部
下村 智昭
歯周病は、腎症、網膜症、神経障害、心疾患、脳卒中に次ぐ糖尿病合併症と言われており、糖尿病患者は歯周病が悪化しやすく、また歯周病が悪化すると血糖コントロールに悪影響を与え、歯周病と糖尿病が相互に負の影響を与えることが報告されております。
例えば、出血や膿を出しているような歯周ポケットからは、炎症に関連した生理活性物質であるサイトカインが、血管を経由して体中に放出されています。
歯周病中等度以上つまり4㎜~7㎜程度の歯周ポケットが口腔内全体にある場合、そのポケット表面積の合計は掌(てのひら)と同じ程度と考えられています。歯周ポケットの中身は外からはなかなか見えませんが、手のひらサイズの出血や膿が治療なしで放置されていると考えると、からだ全体からも無視できない問題であることが理解できると思います。
ポケットから出て、血流にのったサイトカインは、体のなかで血糖値を下げるインスリンを効きにくくします(インスリン抵抗性)。そのため、糖尿病が発症・進行しやすくなるのです。ですから、歯周病をコントロールできればインスリン抵抗性が改善し、血糖コントロールを改善する一つの要因となることが、日本での研究を含めた多くの臨床研究で報告されています。
以上を踏まえまして、糖尿病患者で歯周病を有している方をかかりつけ歯科医に「診療情報提供文書」を添えてご紹介していただき、歯科医療機関(かかりつけ歯科医院)での歯周病治療を行うことで歯周病が改善し、その結果血糖コントロールが改善され、先生方の糖尿病治療の一助となれればと考えております。
歯周病を有している患者とは、以下の項目を自覚される方とお考え下さい。
このような症状を自覚される方は、歯周病が悪化している可能性があります。
医科歯科の連携をうまくとることで、糖尿病と歯周病の双方が改善されればと考えております。さらに、保険診療における歯周病治療において、先生方からの情報提供をいただいた糖尿病患者であれば、3カ月に1度しか行えない処置が毎月行える優遇もあり、一般患者より手厚い治療が可能となっています。(現在、歯科に通院中の患者であってもお手数ですが診療情報提供文書を発行していただく必要があります。) このように、先生方と医科歯科連携を強化し糖尿病の重症化を防げれば幸いです。
医療機器の進歩とともに皮下間質液のグルコース濃度を持続的に測定する持続血糖モニタリング(continuous glucose monitoring, CGM)が可能となり、日常診療で使用できるようになってきました。
アボット社のFreeStyleリブレは、センサーを装着している人が間欠的にリーダーでセンサーをスキャンしてその時の皮下間質液のグルコース濃度測定をする間歇スキャン式CGM(intermittently scanned continuous glucose monitoring、isCGM)です。較正が不要で14日間連続で使用でき、リアルタイムCGMよりも安価で簡便であることから多くの症例で利用されており、血糖変動に関する貴重な情報が得られるデバイスの一つといえます。
ただし、本機でスキャンされて表示される数値はあくまで間質液のグルコース濃度から推測される血糖値ですので、この数値だけに頼ってインスリン量の調整をすることのリスク には留意が必要です。実際、血糖変動が大きいときには間質液のグルコール濃度は血糖変動よりも10~15分遅れることもあります。精度面でもSMBG機器と同等とはいえずSMBG による血糖確認も必要です。以上の注意点をよく認識した上で使用しなければなりません。
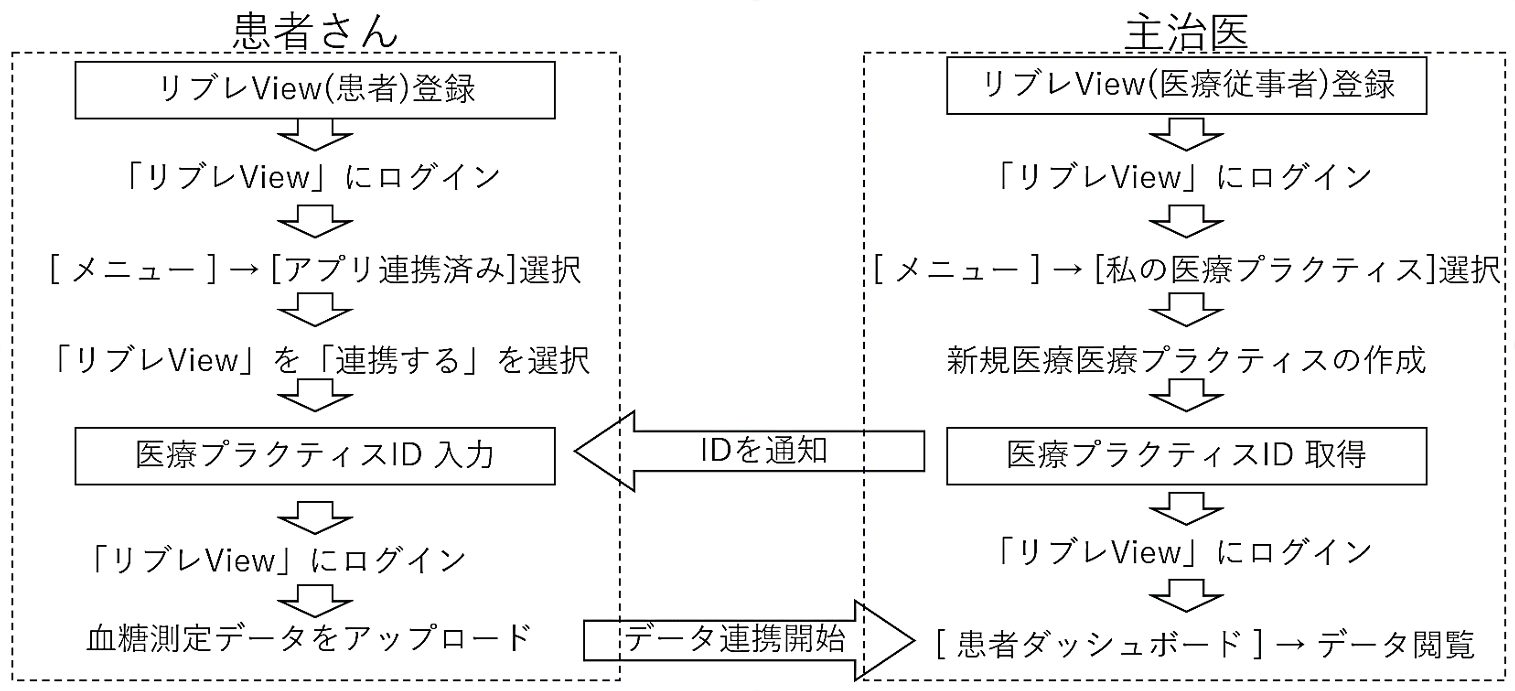
さて、近年はクラウドでのデータ管理も進歩し、FreeStyle リブレに記録されたデータをクラウドベースの管理システムである「リブレView」で管理できるようになっています。各々の医療機関のIDである「医療プラクティスID」を患者さんが入力すれば、医療者がWEB上で患者さんのデータを閲覧できるようになります。大まかな流れは下図の通りです。
また、これまでスキャンはFreeStyleリブレ本体のみでしかできませんでした。実は、FreeStyle リブレのスキャン方式はNFC(近距離無線通信、Near Field Communication)という携帯電話のタッチ決済等に利用されている方式です。2021年2月よりNFC機能を有する携帯電話であればFreeStyle リブレLinkというスマートフォンアプリをインストールしてスキャンできるようになりました(表)。携帯電話でスキャンできると、患者さんはより簡便にかつ人目を気にすることなく血糖のモニタリングが可能となります。

新しいセンサーを装着時にスマートフォンとリンクさせるときには注意点があります。基本的にセンサーは、FreeStyle リブレ本体、スマートフォン両方でスキャン可能なのですが、新しいセンサーを装着する際は、必ずFreeStyle リブレ本体で起動した後に、スマートフォンのFreeStyleリブレLinkアプリで起動するようにしてください。逆の順番で起動すると、スマートフォンではスキャンできても、FreeStyle リブレ本体には反応しなくなります。
以上のようにリブレView、そしてスマートフォンアプリ等を用いて簡便に血糖データ連携できますので、血糖コントロールが難しい症例だけではなくコロナウイルス感染拡大下での遠隔診療にも役に立つと思います。
(文責:豊田 健太郎)
京都糖尿病医会会長
鍵本 伸二
毎年誕生日前後に人間ドックを受けているのですが、2020年は3月のコロナウイルス感染第一波のさなかになりました。感染予防に苦労されている様子をヒシヒシと感じながらドックを終えたところ、腹囲86cm、血圧132/86でメタボリック症候群予備軍と判定されてしまいました。
困った、患者さんに顔向けできない。
医師国保から保健指導を受けなさいと連絡が来るのもなんだか悔しいぞ。
そうだ、医師国保から連絡が来る前にメタボ予備軍を脱出してしまって、出し抜いてやろう!
と、脱メタボ作戦を計画しました。
保健指導の資料にはよく「脂肪を1kg減らすにはエネルギーバランスを7200kcalマイナスにする必要がある」と書かれています。この7200kcalを食事と運動に振り分けて、「食事を1日240kcal減らしたら1ヶ月で7200kcalになり、脂肪を1kg減らせます」とか、「食事を毎日160kcal減らしたら1ヶ月で4800kcal、これに週3日200kcal分の運動を組み合わせたら運動の分が200kcalx3回x4週=2400kcal、合計で7200kcalになり1kg減量できます」という指導を行っています。
しかし残念ながら、この計算通りに減量できた患者さんをあまり見たことがありません。先生方のところでは如何でしょう。当院での指導が下手なのか、それともこの計算が間違っているのか、悩んだことはありませんでしょうか。というわけで、運動でエネルギーを消費して計算通りに体重が減るか、自分の身体で実証実験してみることにしました。
ちょうど新型コロナウイルス感染第1波のさなかで、いろんな会議や研究会が中止になり、受診者も減ったため午前診が定時で終われる日が増えて、時間に余裕が出来ていました。運動の手段は自転車です。元々は自転車が趣味だった訳ではなく、その前年にたまたま衝動買いした折りたたみ小径車(ミニベロ)にはまって、走るのが楽しくなっていました。山が好きなので山の中を走れば運動の効率も上がり密も避けられて、一石二鳥です。
これらを合計すると上の目標(1ヶ月9600kcal)をクリアできることになり、食べる量が今まで通りならば、3ヶ月で4kg減量できるはずです。「運動で減らせるか」の検証なので飲食は極力今まで通りにすることにして、外食が減った分は頑張って家飲みを心がけました。
3月末にチャレンジを開始してから6月まで、木曜土曜の午後には京見峠~持越~雲ヶ畑、貴船~芹生峠、鞍馬~花脊峠、江文峠~大原などの往復約30kmコース、日曜には百井~大見~尾越、保津峡~周山、途中越~琵琶湖など往復60km~80kmコースを走り回りました。
それ以外の平日は昼食後に時間の余裕があればエアロバイクを漕ぎ、最初は限られた時間でなかなか400kcalを達成できませんでしたが、徐々に体力がついてきたのか途中からは180~200ワットで漕ぎ続けて30分程度で400kcalを消費できるようになりました。エアロバイクばかりだと飽きるので、天気の良い日は本物の自転車で京見峠まで往復しています。私の脚でクリニックから往復ほぼ40分で、だいたい400kcal位消費できている計算です。
これを3か月続けたところ6月末には目標の4kg減量を達成、腹囲も82cmまで縮んでめでたくメタボ予備軍を脱出できました。運動での消費エネルギーは推計値であまり正確ではありませんが、保健指導で使っている計算が間違ってはいないことも実感できました。


審査は病名と検査・処方といったレセプトの限られた情報から、診療行為が保険診療のルール(療養担当規則、診療報酬点数表等)と照らし合わせ、適正であるかどうかを確認する作業です。今年度は診療報酬改定の年ではなかったので、審査会の情報として特に最近変わったルールができたわけではありませんので、いくつか順不同で気になることを記載させていただきます。
レセプトを作る作業も大変かと思いますが、今後も、速やかな審査へのご協力をよろしくお願いします。
(文責:小暮 彰典)